|
Zur Hydrologie des Süßwasser-Aquariums |

|
Aquaristik:
Die Grundlagen verstehen
1. ANORGANISCHE ASPEKTE
d. Spuren-Ionen
Struktur
Pourbaix-Bereiche
Eisen und Mangan
Relationen
"Minimum-Tonne"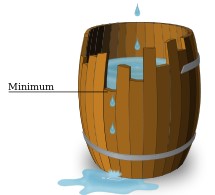 das Analogon
das Analogon
Lücken sind nicht durch andere Stoffe schließbar, Übersättigung wirkungslos


Säuregrad und Redox-Potential
Das "Redox-Potential" ist die Fähigkeit des Wassers, Stoffumwandlungen vorzunehmen,
und wird als "Redox-Spannung" elektrisch gemessen.
Haupteinflussfaktor ist die Sauerstoff-Konzentration (s. "Sauerstoff").
Näheres im Kapitel "Gase" unter "Sauerstoff",
hier soll verwiesen werden auf die besondere Bedeutung für die Spuren-Ionen.

Eisen und Mangan
Fe++ : Mn++ = 2 : 1
Ein Eisen-Dünger ohne entsprechenden Mangan-Zusatz ist weitestgehend wirkungslos.


Relationen


1. ANORGANISCHE ASPEKTE
d. Spuren-Ionen
Struktur
Pourbaix-Bereiche
Eisen und Mangan
Relationen
In
natürlichem Wasser schwirren noch weit mehr Ionen vieler Elemente herum
- allerdings in ganz geringen Mengen, weshalb sie als Spuren-Ionen
bezeichnet seien.Obwohl nur in äußerst geringen Konzentrationen
vorhanden, sind sie für
alle Lebewesen von großer spezifischer Bedeutung. Bei Mangel müssen sie
zwingend gesondert zugeführt werden. Da eine Unterkonzentration gerade
bei
Pflanzen ins Auge sticht, bezeichnet man die Zugabe auch als "düngen",
aber ihre Verfügbarkeit ist für alle anderen Lebewesen im Wasser von
ebensolcher Bedeutung. Deshalb sind diese Stoffe mehr als nur Dünger,
sie gehören wie die bisher besprochenen Ionen zur
Struktur gesunden, naturnahen Wassers.
Wikipedia nennt "für das Wachstum von Grünpflanzen ... 17 chemische Elemente erforderlich". Neben den schon genannten
Die meisten Dünger-Hersteller beschränken sich auf wenige Zusätze, weit vollständiger und sehr naturnah ist diese Vervollständigung des Gessner-Wassers:
"... Kohlenstoff (C), Wasserstoff (H), Sauerstoff (O), Stickstoff (N),
Phosphor (P), Kalium (K), Magnesium (Mg), Calcium (Ca), Schwefel (S)..."
auch nochPhosphor (P), Kalium (K), Magnesium (Mg), Calcium (Ca), Schwefel (S)..."
"... Mangan (Mn), Zink (Zn), Eisen (Fe), Kupfer (Cu),
Bor (B), Chlor (Cl), Molybdän (Mo) und Nickel (Ni)."
Bor (B), Chlor (Cl), Molybdän (Mo) und Nickel (Ni)."
Die meisten Dünger-Hersteller beschränken sich auf wenige Zusätze, weit vollständiger und sehr naturnah ist diese Vervollständigung des Gessner-Wassers:
Spuren-Struktur


Auch
diese Struktur unterliegt der Gesetzmäßigkeit des
"Minimum-Gesetzes" (s.u.), wonach die - möglichst abgestimmte - Vollständigkeit erforderlich
ist. Diese Abstimmung ist in praxi kaum erreichbar, denn es sind
Es bleibt dann nur,
wodurch teilweise Übersättigungen unvermeidbar, in diesen Mengen aber auch unschädlich ist.
- die Relationen wenig bekannt,
- die Konzentrationen nur schwer messbar.
- die Konzentrationen nur schwer messbar.
- Effektivität vor Effizienz zu setzen,
- die Vollständigkeit in ausreichender Konzentration zu erreichen,
- die Vollständigkeit in ausreichender Konzentration zu erreichen,

Das fundamentale Gesetz, das auch alle anderen bisher behandelten Strukturen regiert, ist das
Minimum-Gesetz für das hier Wikipedia zitiert sei:
Das Minimumgesetz (... von Carl Sprengel 1828 veröffentlicht, von Justus von Liebig ... popularisiert) besagt, dass das Wachstum von Pflanzen durch die im Verhältnis knappste Ressource (Nährstoffe wie Kohlenstoffdioxid, Wasser, Licht etc.) eingeschränkt wird. Diese Ressource wird auch als Minimumfaktor bezeichnet. Bei Vorliegen eines solchen Mangelfaktors gibt es keinen Einfluss auf das Wachstum, wenn eine Ressource hinzugegeben wird, die bereits im benötigten Umfang vorhanden ist. Das Minimumgesetz von Carl Sprengel ist unter anderem eine wichtige Grundlage bei der Düngung... | Carl Sprengel ... begründete das Minimumgesetz in der Mineraltheorie „...denn es ist nicht zu bestreiten, wenn eine Pflanze 12 Stoffe zu ihrer Ausbildung bedarf, so wird sie nimmer aufkommen, wenn nur ein einziger an dieser Zahl fehlt, und stets kümmerlich wird sie wachsen, wenn einer derselben nicht in derjenigen Menge vorhanden ist, als es die Natur der Pflanze erheischt“... | Als Modell des Gesetzes fungiert die Faßregel, illustriert als „Minimum-Tonne“: Eine Tonne mit unterschiedlich langen Dauben lässt sich nur bis zur Höhe der kürzesten Daube füllen. Genauso kann ein Organismus sich nur so weit entwickeln, wie es die knappste Ressource erlaubt. |
"Minimum-Tonne"
 das Analogon
das AnalogonLücken sind nicht durch andere Stoffe schließbar, Übersättigung wirkungslos


Da
die Konzentrationen so verschwindend niedrig sind und so schwankend,
bleibt in der Aquaristik kaum etwas Anderes möglich, als eine
größtmögliche Vielfalt, wie oben abgestimmt, großzügig
einzusetzen, zumal ein Überschuss an Spuren-Ionen bei weitem nicht so
kritisch ist wie bei den Neben-Ionen - ausgenommen die unten
beschriebenen Fe- und Mn-Ionen!
Bei den Analysen zu diesem Beitrag wurden ganze drei Produkte gefunden, die den Anforderungen genügen könnten:
Eines wurde inzwischen aufgegeben., die übriggebliebenen werden bei der Düngung der Wasserpflanzen vorgestellt.
Wenngleich die Spuren-Ionen zumeist mit den Neben-Ionen als Pflanzendünger geführt werden,
sind sie - wie eingangs betont -
auch für alle Tiere lebensnotwendig!
Eines wurde inzwischen aufgegeben., die übriggebliebenen werden bei der Düngung der Wasserpflanzen vorgestellt.
Wenngleich die Spuren-Ionen zumeist mit den Neben-Ionen als Pflanzendünger geführt werden,
sind sie - wie eingangs betont -
auch für alle Tiere lebensnotwendig!
Die
Spurenelemente, zumeist Metalle, verbinden sich mit körpereigenen
Enzymen zu Kohle-Wasserstoff-Verbindungen, welche den Stoffwechsel
kontrollieren. Der Bedarf für die Lebewesen im Wasser ist nicht
hinlänglich erforscht. Sicher ist:
Ohne Spurenelemente kein Stoffwechsel!

Die Stabilität gerade der Spuren-Ionen, die für das Wohlergehen von Wasser-Flora und -Fauna unerlässlich sind, hängt ab von
Protonen- und Sauerstoff-Konzentration, i.e.Säuregrad und Redox-Potential
Das "Redox-Potential" ist die Fähigkeit des Wassers, Stoffumwandlungen vorzunehmen,
und wird als "Redox-Spannung" elektrisch gemessen.
Haupteinflussfaktor ist die Sauerstoff-Konzentration (s. "Sauerstoff").
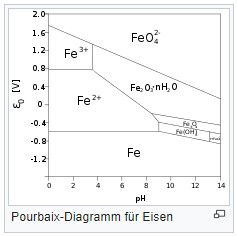
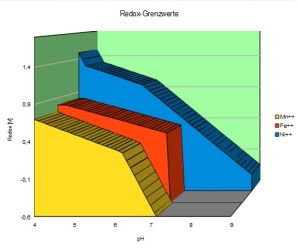
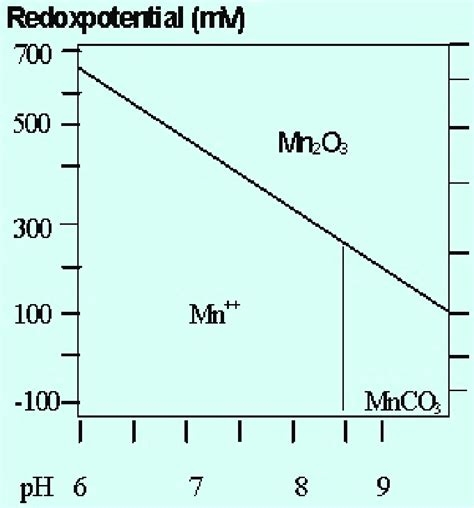
Diese Zusammenhänge wurden von dem belgischen Chemiker Marcel Pourbaix entdeckt, seine Diagramme, "Pourbaix-Diagramme"
genannt, zeigen die Umwandlungen vieler Elemente im pH-Redox-Feld, so
dass deutlich wird, in welchen Bereichen die bestimmten Verbindungen
erhalten bleiben, ohne sich umzuwandeln und damit wertlos zu werden oder
gar einfach auszufallen.
Als Beispiel sei das Element "Eisen Fe" gezeigt, wo das Fe--_Feld im üblichen Süßwasser schon nicht mehr erscheint, sondern die Oxidaton zu Fe2O3 erfolgt.
Als Beispiel sei das Element "Eisen Fe" gezeigt, wo das Fe--_Feld im üblichen Süßwasser schon nicht mehr erscheint, sondern die Oxidaton zu Fe2O3 erfolgt.

Näheres im Kapitel "Gase" unter "Sauerstoff",
hier soll verwiesen werden auf die besondere Bedeutung für die Spuren-Ionen.

Eisen und Mangan
Die
zwei-wertigen Eisen- und Mangan-Kationen, Fe++ und Mn++, sind für alle
Lebewesen im Wasser, besonders deutlich für die Wasserpflanzen, von
großer Bedeutung, da ein Mangel zu erheblichen Schäden führt.
Es kommt hinzu, dass beide in Konkurrenz stehen, sich gegenseitig
verdrängen und ersetzen, wenn ihre Konzentrionen nicht im natürlichen Massen-Verhältnis stehen:
Fe++ : Mn++ = 2 : 1
Ein Eisen-Dünger ohne entsprechenden Mangan-Zusatz ist weitestgehend wirkungslos.



Beide
Ionen sind im Pourbaix-Feld (s.o) recht instabil, besonders das
zwei-wertige Fe++ gibt schnell ein drittes Elektron ab und wandelt sich
damit um zum unbrauchbaren drei-wertigen Fe+++, oder es oxidiert zu
wasserunlöslichen Verbindungen, die dann ausfallen - und das auch in
dem für Süßwasser-Aquarien üblichen Bereich. Das Mangan-Ion Mn++ ist
nicht ganz so instabil, muss aber - entgegen anderer Auffassungen -
ebenso zwingend durch Chelatieren geschützt werden.
Leider werden Mn-Chelate seltener erzeugt.
Leider werden Mn-Chelate seltener erzeugt.

Relationen
Die Ionen, die Pflanzengewässern in gut messbaren Konzentrationen vorkommen,
stehen - wie schon dargelegt - in folgenden Relationen:
stehen - wie schon dargelegt - in folgenden Relationen:
NO3 : Fe = 200 : 1
NO3 : Mn = 400 : 1
Fe : Mn = 2 : 1
NO3 : Mn = 400 : 1
Fe : Mn = 2 : 1


Neumünster, 10.12.2022 *
Egbert W Gerlich *
egbert@ew-gerlich.de