|
Zur Hydrologie des Süßwasser-Aquariums |

|
Aquaristik:
Die Grundlagen verstehen
1. ANORGANISCHE ASPEKTE
c. Neben-Ionen
Stickstoffe
Phosphor
Redfield-Relationen
Pflanzenwachstum
(zu Kalium unten)

Stickstoffe
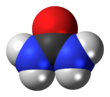
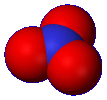

H4N2CO NO3- NH4+
[die gelbe Lücke zeigt das hier fehlende Elektron]
weiterhin auch die daraus abgebauten
Nitrit Ammoniak


NO2- NH3
So, wie der Kohlenstoff die Kohlehydrate und Fette regiert, bestimmt Stickstoff die Proteine, alle drei Nährstoffbereiche bilden mit Wasser nahezu vollständig die Körpersubstanz der hier interessierenden Flora und Fauna - die Konzentration verwertbarer Stickstoffverbindungen ist also ebenso bedeutungsvoll wie das Vorhandensein von Kohlenstoff. Nitrit NO2- und Ammoniak NH3 sind nicht nur nicht verwertbar, sondern schädigend, also - falls vorhanden - vollständig zu eliminieren.
Als Stickstoff-Lieferanten kommen im wesentlich in Frage - wenn wir von der direkten Einvernahme von Tier-/Pflanzensubstanz absehen - Moleküle/Ionen von
Urea - Nitrat - Ammonium
als N-Lieferanten
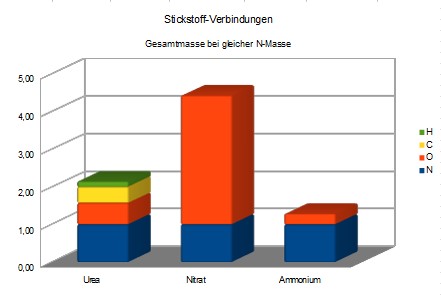
N2H4CO NO3- NH4+

K3 PO4 - K2 HPO4 - K H2PO4

Redfield-Relationen
1x PO4--- 16x NO3- 106x CO2
Durch Multiplikation mit den spezifischen Molekül-Massen ergeben sich folgende

Pflanzenwachstum
sind aufgebaut aus
1x PO4, 16x NO3, 106x CO2, 132x H2O
wobei (4+48+212+22)x O = 143x O2 ins Wasser zurückgeführt werden
Ich nenne sie die
"REDFIELD-Masse-Relationen"
[kg / g / mg]
1xPO4 : 16xNO3 : 106xCO2 : 132xH2O {abzgl 143x O2} = 95 : 992 : 4.665 : 2378 {abzgl 4576 .....}
PO4 : NO3 : CO2 : H2O = 1 : 10,5 : 49,1 : 23,3 {abzgl 48,2}
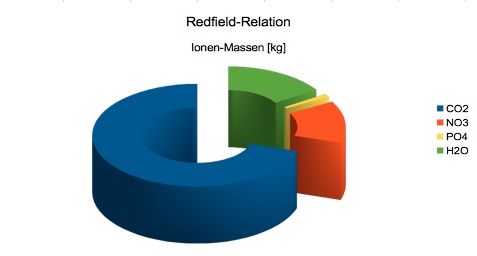

Es kann ein Pflanzenwachstum erzielt werden bei
Sauerstoff-Rückführung von ~ 50 [mg/l]

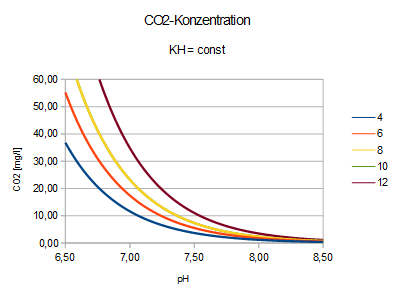
CO2 = Fkt[pH,KH]
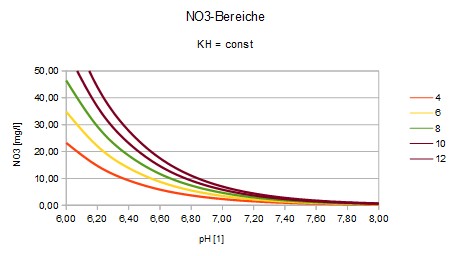
NO3 < 1/5 CO2
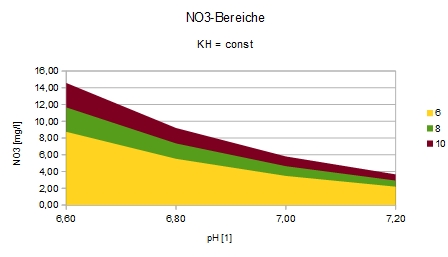
Optimale Nebenionen-Konzentration ist abhängig vom Kohlendioxid-Gehalt, also primär vom pH-Wert!


1. ANORGANISCHE ASPEKTE
c. Neben-Ionen
Stickstoffe
Phosphor
Redfield-Relationen
Pflanzenwachstum
In
diese Gruppe gehören Stoffe, die in natürlichem Wasser in
nennenswerten, wechselhaften Mengen vorkommen, ohne zu den das
Süßwasser definierenden Haupt-Ionen zu gehören - streng genommen sind
es Verunreinigungen des reinen Wassers. Ihre Bedeutung liegt vor allem
darin, dass Wasserpflanzen aus ihnen ihre Biomasse bilden, wodurch sie
unerlässlich sind in Pflanzengewässern. Es sind dies Verbindungen von
Stickstoff N, Phosphor P und Kohlenstoff C sowie Kalium(zu Kalium unten)

Stickstoffe
Stickstoff
als prägendes Element der Proteine ist von größter Bedeutung für nahezu
alle Lebewesen, machen doch Proteine etwa die Hälfte der
Zell-Trockenmasse aus. Wegen des Stickstoff-Gehalts können Proteine
("Eiweiß") auch nicht durch Kohlehydrate oder Fette ersetzt werden, die ja kein Stickstoff enthalten. Hier
von besonderem Interesse sind Stickstoffverbindungen, die für den
Stoffwechsel von Flora und Fauna natürlichen Wassers notwendig sind.
Als Verwesung- und/oder Ausscheidungsprodukte, als Überreste tierischer oder pflanzlicher Proteine ("Eiweiße"), schwirren durch natürliches Wasser die Stickstoff-Verbindungen
Urea ("Harnstoff")
Nitrat
Ammonium
Als Verwesung- und/oder Ausscheidungsprodukte, als Überreste tierischer oder pflanzlicher Proteine ("Eiweiße"), schwirren durch natürliches Wasser die Stickstoff-Verbindungen



H4N2CO NO3- NH4+
[die gelbe Lücke zeigt das hier fehlende Elektron]
weiterhin auch die daraus abgebauten
Nitrit Ammoniak


NO2- NH3
Modelle https://en.wikipedia.org/wiki/Ammonia ff
So, wie der Kohlenstoff die Kohlehydrate und Fette regiert, bestimmt Stickstoff die Proteine, alle drei Nährstoffbereiche bilden mit Wasser nahezu vollständig die Körpersubstanz der hier interessierenden Flora und Fauna - die Konzentration verwertbarer Stickstoffverbindungen ist also ebenso bedeutungsvoll wie das Vorhandensein von Kohlenstoff. Nitrit NO2- und Ammoniak NH3 sind nicht nur nicht verwertbar, sondern schädigend, also - falls vorhanden - vollständig zu eliminieren.
Als Stickstoff-Lieferanten kommen im wesentlich in Frage - wenn wir von der direkten Einvernahme von Tier-/Pflanzensubstanz absehen - Moleküle/Ionen von
Urea - Nitrat - Ammonium
als N-Lieferanten

N2H4CO NO3- NH4+
deren
Stickstoff-Anteil hier im Massen-Vergleich dargestellt ist. Der
stärkste N-Lieferant ist Urea, das von Tieren im Urin ausgeschieden
wird, das aber auch den komplexesten Umwandlungsprozess durchläuft.
Die kritische Umwandlung von NH4+ in NH3 in alkalischem Wasser wurde schon besprochen wie auch die Bedeutung des pH-Wertes für die Bildung von Salpetriger Säure (Basisionen II)
Die kritische Umwandlung von NH4+ in NH3 in alkalischem Wasser wurde schon besprochen wie auch die Bedeutung des pH-Wertes für die Bildung von Salpetriger Säure (Basisionen II)

Die Umwandlung der Stickstoff-Verbindungen ist ein bio-chemischer, um nicht zu sagen "biologischer" Prozess, weshalb er bei den biologischen Aspekten noch zu beleuchten ist. Chemisch geschieht Folgendes:
Bei Vorhandensein jeweils bestimmter Mikro-Organismen und bei jeweils bestimmter Sauerstoff-Konzentration ("Redox-Potential")
(NH3 + p+) + 2*O2 + e- = NO2- + 2*H2OBei Vorhandensein jeweils bestimmter Mikro-Organismen und bei jeweils bestimmter Sauerstoff-Konzentration ("Redox-Potential")
wird Urea N2H4CO zersetzt zu Ammonium NH4+ und Ammoniak NH3
N2H4CO + H2O = NH4+ + NH3 + HCO3
N2H4CO + H2O + p+ = 2*NH4+ + HCO3-
N2H4CO + H2O + p+ = 2*NH4+ + HCO3-
werden Ammonium NH4+ und Ammoniak NH3 beim Stoffwechsel oxidiert zu Nitrit NO2-
wird vorhandes Nitrit NO2- beim Stoffwechsel oxidiert zu Nitrat NO3-
2*NO2- + O2 = 2*NO3-Dieses
NO3-, aber ersatzweise auch NH4+, wird von Pflanzen schnellstmöglich in neue Bio-Masse eingebaut - das Ganze wird besungen als
"Stickstoff-Kreislauf"
N2H4CO => 2*NO3- + H2CO3 + H2O
N2H4CO => 2*NO3- + H2CO3 + H2O
(was durch die H2CO3-Dissoziation bekanntlich zur Ansäuerung führt - zudem werden 4,5*O2 verbraucht), wobei
zu betonen ist, dass diese Umwandlungen nur möglich sind, soweit
die für jede Stufe
notwendigen Mikro-Organismen
hinlänglich zur
Verfügung stehen - und zwar im aeroben Umfeld, also Sauerstoff-Überschuss
In saurem Wasser entsteht praktisch kein Ammoniak und deshalb kein Nitrit, aber
bei Sauerstoff-Mangel, also bei niedriger Redox-Spannung, und
durch Photolyse bei UV-Bestrahlung kann sich dieser hilfreiche Prozess umkehren, und aus Nitrat wird gefährliches Nitrit
bei Sauerstoff-Mangel, also bei niedriger Redox-Spannung, und
durch Photolyse bei UV-Bestrahlung kann sich dieser hilfreiche Prozess umkehren, und aus Nitrat wird gefährliches Nitrit
2* NO3- = 2* NO2- + O2
2*NO3- = N2 + 3*O2
2*NO2- = N2 + 2*O2
2*NO3- + 6*H+ = N2 + 3*O2

Das Kohlenstoff-System wird regiert von den Protonen (pH-Wert),
das Stickstoff-System von Bakterien!


Phosphor
Phosphat-Ion
PO4---
diffundiert beispielsweise aus der Phosphorsäure
H3PO4 = PO4--- + 3*H+
Überschüssiges, also nicht von
Pflanzen aufgenommenes Nitrat und Nitrit kann von anderen
Mikro-Organismen verarbeitet werden zu den Gasen
Stickstoff N2 plus Sauerstoff O22*NO3- = N2 + 3*O2
2*NO2- = N2 + 2*O2
Das wird noch zu erwähnen sein beim Sauerstoff und der Wasserbiologie...


Achtung: Es verarbeiten anaerobe Bakterien in anaerobem Umfeld, also bei Sauerstoff-Mangel,
Nitrat zu Stickstoff und Sauerstoff2*NO3- + 6*H+ = N2 + 3*O2
Durch den Protonenverbrauch steigt der pH-Wert...

Das Kohlenstoff-System wird regiert von den Protonen (pH-Wert),
das Stickstoff-System von Bakterien!


Phosphor
Beim Aufbau von organischen
Zellen, für Pflanzen und Tiere, spielt das Element Phosphor eine
wichtige Rolle. Im Wasser steht es besonders den Pflanzen zur Verfügung
als
Phosphat-Ion

PO4---
diffundiert beispielsweise aus der Phosphorsäure
H3PO4 = PO4--- + 3*H+
Ein Phosphat-Mangel kann durch Zugabe von Phosphorsalzen, den Phosphaten, schnell behoben werden, am sinnvollsten durch die Kalium-Phosphate
K3 PO4 - K2 HPO4 - K H2PO4
Das wird bei der Planzendüngung erläutert werden.

Redfield-Relationen
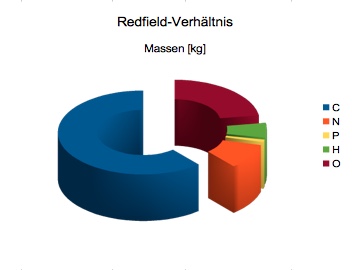
Bei der Untersuchung marinen Phytoplanktons erkannte Alfred C. Redfield einen Zusammenhang des atomaren Gehalts von
Kohlenstoff C : Stickstoff N : Phosphor Pder nach ihm als "Redfield-Verhältnis"
("Redfield Ratio") bezeichnet wurde. Unstrittig für die Meeresbiologie,
ist diese Theorie hilfreich auch für die
Süßwasser-Flora, wenngleich nicht ausreichend untersucht. Analoges gilt für die Buddendorf'sche Algentheorie, wonach eine Algenblüte von unnatürlicher N:P-Relation geprägt sei (s.u. ! ).
Demnach werde die Ausbreitung gefördert


Die betreffenden Elemente sind im Wasser wesentlich enthalten in den Anionen von
Phosphat, Nitrat und Kohlendioxid:Demnach werde die Ausbreitung gefördert
("Algenblüte")
von Cyanobakterien ("Blaualgen") bei Phosphat-Überschuss
von (Grün-) Algen bei Phosphat-Mangel
NO3 : PO4 >> 10 führe zu Grün-Algen
von Cyanobakterien ("Blaualgen") bei Phosphat-Überschuss
von (Grün-) Algen bei Phosphat-Mangel
Also (s.u. ! ):
NO3 : PO4 << 10 führe zu Blau-AlgenNO3 : PO4 >> 10 führe zu Grün-Algen


Nach Redfield kommen im Phytoplankton auf
1x P-Atom
16x N-Atome, 106x C-Atome, 264x H-Atome, 110x O-Atome
als Masse ausgedrückt
1.528[g] + 2.025[g] = 3.553[g]
Solange
das Wasser in genügenderMenge zur Verfügung steht - wie im Aquarium -,
kann es zunächst unberücksichtigt bleiben, deshalb16x N-Atome, 106x C-Atome, 264x H-Atome, 110x O-Atome
als Masse ausgedrückt
1.528[g] + 2.025[g] = 3.553[g]

1x P-Atom 16x N-Atome 106x C-Atome
P : N : C = 1 : 16 : 106
P : N : C = 1 : 16 : 106
Die betreffenden Elemente sind im Wasser wesentlich enthalten in den Anionen von
1x PO4--- 16x NO3- 106x CO2
Durch Multiplikation mit den spezifischen Molekül-Massen ergeben sich folgende
Masse-Relationen
[kg / g / mg]
1xPO4 : 16xNO3 : 106xCO2 = 95 : 992 : 4.665
PO4 : NO3 : CO2 = 1 : 10,5 : 49,1
[kg / g / mg]
1xPO4 : 16xNO3 : 106xCO2 = 95 : 992 : 4.665
PO4 : NO3 : CO2 = 1 : 10,5 : 49,1
Auf
dem Weg zum "pflanzenfreundlichen Wasser" sind dies Meilensteine:
NO3 : PO4 = 10 : 1  CO2 : NO3 = 5 : 1
CO2 : NO3 = 5 : 1
NO3 = 0,2*CO2
PO4 = 0,02*CO2
 CO2 : NO3 = 5 : 1
CO2 : NO3 = 5 : 1NO3 = 0,2*CO2
PO4 = 0,02*CO2

Pflanzenwachstum
Nehmen wir jetzt den obigen Wassergehalt hinzu:
1x P 16x N 106x C 264x H 110x Osind aufgebaut aus
1x PO4, 16x NO3, 106x CO2, 132x H2O
wobei (4+48+212+22)x O = 143x O2 ins Wasser zurückgeführt werden
Ich nenne sie die
"REDFIELD-Masse-Relationen"
[kg / g / mg]
1xPO4 : 16xNO3 : 106xCO2 : 132xH2O {abzgl 143x O2} = 95 : 992 : 4.665 : 2378 {abzgl 4576 .....}
PO4 : NO3 : CO2 : H2O = 1 : 10,5 : 49,1 : 23,3 {abzgl 48,2}
NO3 : PO4 = 10,5 ~ 10
CO2 : PO4 = 49,1 ~ 50
CO2 : -O2 = 1,02 ~ 1
CO2 : PO4 = 49,1 ~ 50
CO2 : -O2 = 1,02 ~ 1


Es kann ein Pflanzenwachstum erzielt werden bei
CO2 ~ 50 [mg/l]
NO3- ~ 10 [mg/l]
PO4--- ~ 1 [mg/l]
H2O ~ 25 [mg/l]
von ~ 35 [mg/l] bei einer NO3- ~ 10 [mg/l]
PO4--- ~ 1 [mg/l]
H2O ~ 25 [mg/l]
Sauerstoff-Rückführung von ~ 50 [mg/l]
Wasserpflanzen geben fast ebenso viel Sauerstoff ab, wie sie Kohlendioxid verbrauchen.

An dieser Stelle ist ein Element zu ergänzen, das
Redfield unerwähnt gelassen hat, das aber von Pflanzen zum Aufbau ihrer
Masse benötigt wird:
Es gehört, der bisherigen Gliederung folgend, zwar nicht zu den Neben-Ionen, muss aber hier im Hinblick auf die Pflanzenmasse berücksichtigt werden. Bis zu 5 % der Pflanzenmasse bestehen aus Kalium, so dass ergänzend zu erweitern ist:

Es gehört, der bisherigen Gliederung folgend, zwar nicht zu den Neben-Ionen, muss aber hier im Hinblick auf die Pflanzenmasse berücksichtigt werden. Bis zu 5 % der Pflanzenmasse bestehen aus Kalium, so dass ergänzend zu erweitern ist:
Es kann ein Pflanzenwachstum erzielt werden bei
von ~ 37,5 [mg/l] bei einer
Sauerstoff-Rückführung von ~ 50 [mg/l]
CO2 ~ 50 [mg/l]
NO3- ~ 10 [mg/l]
PO4--- ~ 1 [mg/l]
H2O ~ 25 [mg/l]
K+ ~ 1,5 [mg/l]
NO3- ~ 10 [mg/l]
PO4--- ~ 1 [mg/l]
H2O ~ 25 [mg/l]
K+ ~ 1,5 [mg/l]
von ~ 37,5 [mg/l] bei einer
Sauerstoff-Rückführung von ~ 50 [mg/l]

Erinnern wir uns, wie bei bekannter Karbonathärte KH
aus dem pH-Wert die CO2-KonzentrationCO2 = Fkt[pH,KH]

abgeleitet
werden kann, und diese bestimmt, REDFIELD folgend, die optimale
Konzentration der Neben-Ionen für Pflanzengewässer. Die Nitrat-Konzentration soll ein Fünftel der
Kohlendioxid-Konzentration nicht übersteigen:
NO3 < 1/5 CO2


Optimale Nebenionen-Konzentration ist abhängig vom Kohlendioxid-Gehalt, also primär vom pH-Wert!
NO3 = 1/5 CO2
PO4 = 1/50 CO2
CO2 = Fkt[pH]
PO4 = 1/50 CO2
CO2 = Fkt[pH]
Das Diagramm zeigt, dass es keine allgemeine Steuerungs-Empfehlung
geben kann. Auch ist ersichtlich, dass eine höhere Rate des
Pflanzenwachstums tendenziell bei härterem Wasser erreichbar ist,
weil dieses eine höhere CO2-Konzentration ermöglicht (wodurch das
Wasser ansäuert). Wegen des möglichen Nährstoffgehaltes gilt also:
Ein Pflanzenzuchtwasser ist hart und sauer 


Somit kann mittels Tabellenprogramm das
maximal erzielbare Pflanzenwachstum in Abhängigkeit von Säuregrad und Karbonathärte bestimmt werden. Dieses Programm, das gerade auch das Düngungsmaximum darlegt, stelle ich gerne zur Verfügung. 
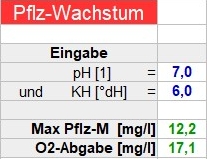
Pflz = fkt [pH, KH]
Das wird bei der Düngung der Wasserpflanzen vorgestellt und berechnet werden.


Pflz = fkt [pH, KH]

Das wird bei der Düngung der Wasserpflanzen vorgestellt und berechnet werden.

Neumünster, 26.04.2025 *
Egbert W Gerlich *
egbert@ew-gerlich.de